129101-37-7
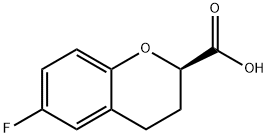 129101-37-7 结构式
129101-37-7 结构式
基本信息
(R)-6-氟-3,4-二氢苯异吡喃-2-甲酸
(R)-6-氟-3,4-二氢苯并吡喃-2-甲酸
(R)-(+)-6-氟-色满-2-羧酸奈必洛尔中间体
(R)-6-氟-3,4-二氢-2H-1-苯并吡喃-2-羧酸
6-Fluorochromane-2-carboxylic acid
(R)-6-FluorochroMan-2-carboxylic acid
(2R)-6-fluorochromane-2-carboxylic acid
(R)-6-Fluoro-3,4-dihydro-2H-1-benzopyran-2-carboxylic acid
(2R)-6-Fluoro-3,4-dihydro-2H-1-benzopyran-2-carboxylic acid
2H-1-Benzopyran-2-carboxylic acid, 6-fluoro-3,4-dihydro-, (2R)-
(2R)-6-Fluoro-2-[(2R)-oxiran-2-yl)-3,4-dihydro-2H – chromene (Isomer - B )
物理化学性质
制备方法

129050-25-5

129101-37-7
一般步骤:在室温下,向搅拌的奈必洛尔杂质35(2a-f)的四氢呋喃(THF,2 mL)和甲醇(MeOH,1 mL)混合溶液中,缓慢滴加0.25 M的氢氧化锂(LiOH)水溶液(1.05当量),持续搅拌2小时。反应完成后,将反应混合物减压浓缩,随后用稀盐酸(HCl)酸化。粗产物用乙酸乙酯(EtOAc)萃取,合并有机相并用无水硫酸镁(MgSO4)干燥。过滤后,减压蒸发溶剂得到粗产物。通过正己烷结晶进一步纯化,得到目标产物6a-f。 4.2.22 (R)-6-氟色满-2-羧酸(6a)的合成:按照4.2.21节所述方法,以2a(100 mg,0.47 mmol)为原料,经过上述一般步骤处理,得到化合物6a(89 mg),收率96%。 1H NMR (δ, ppm): 6.88-6.80 (m, 2H), 6.75 (dd, 3J = 8.7, 4JH-F = 2.6, 1H), 4.74 (dd, 1H, J = 7.6, 3.5), 2.90-2.75 (m, 2H), 2.33 (m, 1H), 2.18 (m, 1H). 13C NMR (δ, ppm): 175.8, 157.2 (d, 1JC-F = 237.9), 148.9 (d, 4JC-F = 2.1), 122.3 (d, 3JC-F = 7.5), 117.8 (d, 3JC-F = 8.1), 115.4 (d, 2JC-F = 22.7), 114.5 (d, 2JC-F = 23.2), 73.2, 24.1, 23.5 (d, 4JC-F = 1.1). 旋光度:[α]D20 = -12.6 (c 1.0, DMF) {文献值 [α]D20 = -13.4 (c 1.0, DMF)}. 对映体过量(ee)> 99%,使用Chiralcel ODH柱,正己烷/2-丙醇/三氟乙酸 = 90:10:0.5为流动相,流速1.0 mL/min,保留时间tR = 6.92 min(S)和9.62 min(R)。 高分辨质谱(HRMS)计算值C10H9FO3 [M]+:196.0530,实测值:196.0531。
参考文献:
[1] Tetrahedron Asymmetry, 2015, vol. 26, # 17, p. 912 - 917
[2] Patent: KR2017/37154, 2017, A. Location in patent: Paragraph 0291-0293
