背景技术
他汀类降血脂药物中最关键药物的阿伐他汀是由美国Warner Lambert开发的他汀类降血脂药物,主要结构构成为母环和手性侧链,目前产品国内市场也是竞争非常激烈。R(-)-4-氰基-3-羟基丁酸乙酯(Ethyl (R)-(-)-4-cyano-3-hydroxybutyate),分子式C7H11NO3,分子量157.17,具有一个带羟基的手性结构,是目前合成第三代他汀类药物的关键中间体,如以它为原料合成的阿托伐他汀(atorvastatin)销售非常火爆,效果也是非常好目前销售额最高接近100亿美元。因此降低原辅料的合成成本和研究新的合成R(-)-4-氰基-3-羟基丁酸乙酯方法一直是国内外关注的热点。

目前开发反应条件更温和更高效并且更加经济环保合成R(-)-4-氰基-3-羟基丁酸乙酯可以通过和醋酸叔丁酯缩合然后酶还原得到血脂药物阿托伐他汀的手性侧链因此此环合物作为阿托伐他汀的关键中间体也是手性合成重要研究课题。目前蛋白质工程技术和酶工程技术发展迅速,酶催化在化学反应在有机合成中特别是手性合成中得到非常广泛的应用。随着酶技术发展,利用酶催化进行化合物的化学合成成为技术革新的重要手段也是复杂化合物技术改进的重要方法,一种新思路化合物的化学-酶法合成的正成为药物以及中间体制备重要手段也取得了很显著的进展。
本文在两步酶法的基础上进行改进提升提出了两步固定化酶催化的更加绿色环保制备R(-)-4-氰基-3-羟基丁酸乙酯的新工艺。该工艺在两步酶催化的基础上进行研究参考了尤忠毓的研究在这个基础上根据多年酶固定化的研究将酮还原酶以及脱氢酶一起固定在树脂上,就是将酶采用环氧树脂进行共固定化,然后用固定化酶进行催化反应。
制备方法
一、固定化酶YKL0210和YKL0212的制备
1.1、YKL0210 的制备:取菌泥K122菌泥20克;K336菌泥30克菌泥和0.1mol的PBS缓冲盐300mL投入500mL 的三口烧瓶中搅拌均匀并冷却降温到4℃~8℃。然后将料液倒入均质机(ATS AH-BASIC30)中控制压力在85±10Mpa,重复二次使菌完全破碎,均质时必须控制物料温度5℃~15℃,絮凝除菌:把配制好的絮凝剂缓慢加入均质液中,搅拌30min 后用多管离心机(ANKEDL-5-B)离心10min以上;取上清液用于备用;控制上清液pH在7.8~8.2之间,如有需要用磷酸氢二钾或者磷酸二氢钾调节pH到要求范围,加入适量的PLP然后再投入树脂50克(LX-028蓝晓环氧树脂)开始搅拌。搅拌控制温度在20℃~25℃固定20h以上 。过滤树脂用纯化水淋洗两遍后抽干得固定化酶YLL-0210备用,检测酶活要求酶活在120以上。
1.2、YKL0212的制备:取菌泥G013菌泥50克;加入0.1mol的PBS缓冲盐300mL投入500mL 的三口烧瓶中搅拌均匀并冷却降温到 4℃~8℃。然后将料液倒入均质机(ATS AH-BASIC 30)中控制压力在85±10Mpa,重复二次使菌完全破碎,均质时必须控制物料温度 5℃~15℃,絮凝除菌:把配制好的絮凝剂缓慢加入均质液中,搅拌30min后用多管离心机(ANKE DL-5-B)离心10min以上;取上清液用于固定化;检测上清液pH在7.8~8.2之间可用磷酸氢二钾或者磷酸二氢钾调节PH到要求范围,加入适量的PLP再投入树脂50克(LX-028蓝晓环氧树脂)开始固定化。搅拌控制温度在20℃~25℃固定20h以上。过滤后树脂用纯化水淋洗两遍后抽干,检测酶活要求酶活在200以上得固定化树脂YKL0212待用。
二、催化反应过程
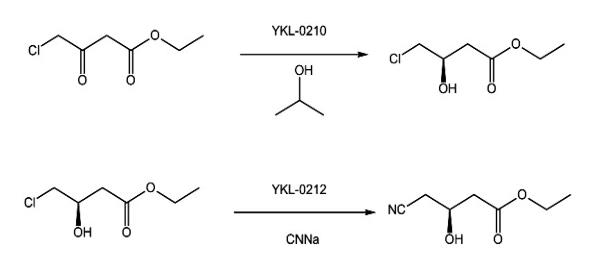
2.1、合成(S)-4-氯-3-羟基乙酯
将300g(2.16mol)4-氯乙酰乙酸乙酯和50mL的0.1mol的PBS以及162.5mL(2.52mol)异丙醇加入1000mL三口烧瓶中,温度控制在室温,加入固定化酶YKL0210(弈柯莱生物科技公司产品酶)50克搅拌均匀,然后缓慢升温到38℃~42℃搅拌反应5小时后温度控制在45℃以下减压蒸出80mL溶剂后再加50mL(0.65mol)的异丙醇继续搅拌0.5小时后再在同样温度下真空蒸馏反应3小时检测反应中4-氯乙酰乙酸乙酯的含量小于0.5%停止反应,过滤除去固定化酶(固定化酶套用),滤液先减压蒸馏除去溶剂然后高真空蒸馏得到291.2g(S)-4-氯-3-羟基丁酸乙酯,摩尔收率为95.87%。比旋度:[α]D25=-14.6°(c1.0;氯仿)(文献值[α]D25=-14.5°(c1.0;氯仿))1HNMR(CDCl3)δ:4.28(m,H),4.2(m,2H),3.62(m,2H),2.64(m,2H),1.30(m,3H)。
2.1、固定化酶的套用
将回收的固定化酶加入1000mL三口烧瓶中加入300g(2.16 mol)4-氯乙酰乙酸乙酯和50mL的0.1mol的PBS以及162.5mL(2.52mol)异丙醇补加PLP溶液2mL后搅拌,然后缓慢升温到38℃~42℃搅拌反应5小时后温度控制在45℃以下减压蒸出80mL溶剂后再加入50mL(约0.65mol)的异丙醇继续搅拌1小时后再真空蒸馏反应3小时检测反应中4-氯乙酰乙酸乙酯的含量小于0.5%停止反应(如果达不到继续补加异丙醇以及继续真空反应),过滤除去固定化酶(固定化酶继续套用),滤液先减压蒸馏除去溶剂然后高真空蒸馏得到产品(S)-4-氯-3-羟基乙酯。
2.3、合成R(-)-4-氰基-3-羟基丁酸乙酯
取200g(1.21mol)(S)-4-氯-3-羟基丁酸乙酯和100mL的0.1mol的PBS溶液和95%乙醇100mL加入1000mL三口瓶中室温下加入固定化酶YKL0212(弈柯莱生物科技公司产品酶)40克;在35℃的滴加液中加入30%的氰化钠200g(1.22mol),滴加过程中用4.0N盐酸调节保持pH=7.8~8.2滴加完毕后在35℃保温,继续反应3小时后降温过滤;固定化酶继续套用使用,滤液加活性炭脱色过滤然后先蒸馏除去溶剂和水,然后再高真空蒸馏得到173.1g R(-)-4-氰基-3-羟基丁酸乙酯,收率为91.8%。气相含量99.38%。比旋度[α]D25=-33.2°(c1.0;氯仿)(文献值[α]D25=-32.5°(c1.0;氯仿))核磁数据:1HNMR(CDCl3)δ:4.38(m,1H),4.20(m,2H),3.74~3.52(m,4H),1.30(m,3H)[1]。
参考文献
[1]徐斌,柴多武,洪治. 手性中间体(R)-4-氰基-3-羟基丁酸乙酯制备工艺改进[J]. 广东化工,2024,51(16):39-41. DOI:10.3969/j.issn.1007-1865.2024.016.013.
