佩米替尼
| 中文名称 | 佩米替尼 |
|---|---|
| 中文同义词 | 培米加替尼;3-(2,6-二氟-3,5-二甲氧基苯基)-1-乙基-1,3,4,7-四氢-8-(4-吗啉基甲基)-2H-吡咯并[3',2':5,6]吡啶[4,3-D]嘧啶-2-酮;帕米加替尼;化合物PEMIGATINIB;培米替尼;3-(2,6-二氟-3,5-二甲氧基苯基)-1-乙基-8-(吗啉代甲基)-1,3,4,6-四氢-2H-吡咯并[3',2':5,6]吡啶并[4,3-D]嘧啶-2-酮;培美加替尼;2H8]-培米加替尼 |
| 英文名称 | Pemigatinib |
| 英文同义词 | Pemigatinib;3-(2,6-difluoro-3,5-dimethoxyphenyl)-1-ethyl-8-(morpholin-4-ylmethyl)-1,3,4,7-tetrahydro-2H-pyrrolo[3',2':5,6]pyrido[4,3-d]pyrimidin-2-one;INCB-054828;3-(2,6-difluoro-3,5-dimethoxyphenyl)-1-ethyl-8-(morpholinomethyl)-1,3,4,7-tetrahydro-2H-pyrrolo[3',2':5,6]pyrido[4,3-d]pyrimidin-2-one;2H-Pyrrolo[3',2':5,6]pyrido[4,3-d]pyrimidin-2-one, 3-(2,6-difluoro-3,5-dimethoxyphenyl)-1-ethyl-1,3,4,7-tetrahydro-8-(4-morpholinylmethyl)-;IBI-375;3-(2,6-Difluoro-3,5-dimethoxyphenyl)-1-ethyl-8-(morpholinomethyl)-1,3,4,6-tetrahydro-2H-pyrrolo[3',2':5,6]pyrido[4,3-d]pyrimidin-2-one;2H8]-Pemigatinib |
| CAS号 | 1513857-77-6 |
| 分子式 | C24H27F2N5O4 |
| 分子量 | 487.5 |
| EINECS号 | |
| 相关类别 | 抑制剂;标准品;医药原料;贝尔卡主打;武汉贝尔卡主打;APIS |
| Mol文件 | 1513857-77-6.mol |
| 结构式 | 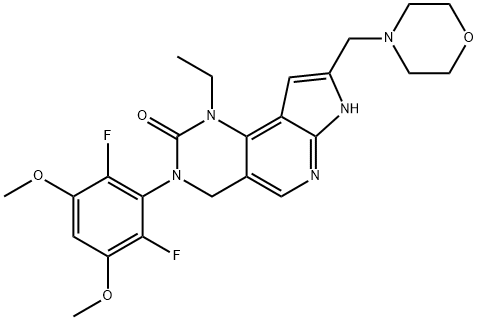 |
佩米替尼 性质
| 沸点 | 697.6±55.0 °C(Predicted) |
|---|---|
| 密度 | 1.44±0.1 g/cm3(Predicted) |
| 储存条件 | Store at -20°C |
| 溶解度 | DMSO:40.0(最大浓度 mg/mL);82.05(最大浓度 mM) |
| 酸度系数(pKa) | 11.56±0.40(Predicted) |
| 形态 | 结晶固体 |
| 颜色 | 白色至浅黄色 |
| InChIKey | HCDMJFOHIXMBOV-UHFFFAOYSA-N |
| SMILES | C1(=O)N(C2=C(F)C(OC)=CC(OC)=C2F)CC2=CN=C3NC(CN4CCOCC4)=CC3=C2N1CC |
佩米替尼片是一种针对FGFR亚型1/2/3的强效选择性口服抑制剂。2022年4月,佩米替尼(中文商标:达伯坦®)获国家药品监督管理局(NMPA)批准,用于既往至少接受过一种系统性治疗,且经检测确认存在有FGFR2 融合或重排的晚期、转移性或不可手术切除的胆管癌成人患者的治疗。达伯坦®由Incyte和信达生物共同开发,信达生物负责中国大陆、香港、澳门和台湾地区的商业化。
2024年4月22日,信达生物制药宣布,达伯坦®(佩米替尼片)在中国澳门获批上市,用于曾接受过全身性治疗后疾病恶化、肿瘤具有FGFR2融合或重排的局部晚期或转移性胆管癌的成人患者。美国FDA和中国国家药品监督管理局(NMPA)分别于2020年4月17日和2022年3月29日,批准佩米替尼(Pemigatinib)用于治疗携带FGFR2融合或重排的经过治疗的、不可切除的晚期、转移性胆管癌患者。NCCN胆道癌指南及中国临床肿瘤学会(CSCO)胆道恶性肿瘤诊疗指南推荐佩米替尼作为FGFR2基因融合或重排胆管癌患者的二线治疗。基于FOENIX-CCA2结果,美国FDA批准福巴替尼(Futibatinib)用于伴有FGFR2基因融合/重排的、先前治疗过的、不可切除的、局部晚期或转移性ICC患者。
2024年4月22日,信达生物制药宣布,达伯坦®(佩米替尼片)在中国澳门获批上市,用于曾接受过全身性治疗后疾病恶化、肿瘤具有FGFR2融合或重排的局部晚期或转移性胆管癌的成人患者。美国FDA和中国国家药品监督管理局(NMPA)分别于2020年4月17日和2022年3月29日,批准佩米替尼(Pemigatinib)用于治疗携带FGFR2融合或重排的经过治疗的、不可切除的晚期、转移性胆管癌患者。NCCN胆道癌指南及中国临床肿瘤学会(CSCO)胆道恶性肿瘤诊疗指南推荐佩米替尼作为FGFR2基因融合或重排胆管癌患者的二线治疗。基于FOENIX-CCA2结果,美国FDA批准福巴替尼(Futibatinib)用于伴有FGFR2基因融合/重排的、先前治疗过的、不可切除的、局部晚期或转移性ICC患者。
佩米替尼通过选择性抑制突变的FGFR2,减少FGFR信号通路的激活,从而抑制肿瘤细胞的增殖、迁移、存活和血管生成,最终抑制肿瘤的生长。
Pemigatinib (INCB054828, Pemazyre)是一种口服活性的 FGFR 的选择性抑制剂,对于FGFR1、FGFR2、FGFR3和FGFR4的IC50分别为0.4 nM、0.5 nM、1.2 nM和30 nM。Pemigatinib(INCB054828)具有治疗胆管癌的潜力。| Target | Value |
|
FGFR1
(Cell-free assay) | 0.4 nM |
|
FGFR2
(Cell-free assay) | 0.5 nM |
|
FGFR3
(Cell-free assay) | 1.2 nM |
|
FGFR4
(Cell-free assay) | 30 nM |
佩米替尼已获得USFDA批准,用于治疗胆管癌的口服药物。
在化合物284中酸性条件下去除乙醛保护基,得到醛285。醛285与苯胺286进行还原胺化反应,生成苯甲基胺287。苯甲基胺287与异氰酸酯288反应,形成预期的尿289。在强碱LHMDS(锂双甲基硅烷)的作用下,化合物289发生分子内环化反应,取代邻近的氯原子,生成氮杂三环化合物290。通过常规水解去除苯磺酰基团,完成佩米替尼的构建,得到良好产率的最终产物。

安全信息
| 更新日期 | 产品编号 | 产品名称 | CAS号 | 包装 | 价格 |
|---|---|---|---|---|---|
| 2026/03/03 | S0088 | 培米加替尼 Pemigatinib (INCB054828) | 1513857-77-6 | 2mg | 1220.31元 |
| 2026/03/03 | S0088 | 培米加替尼 Pemigatinib (INCB054828) | 1513857-77-6 | 5mg | 2285.01元 |
