背景技术
糖基化反应通常是由糖基转移酶催化的,尿嘧啶核苷二磷酸(UDP)‑葡萄糖依赖的糖基转移酶是目前应用最多的糖基转移酶之一。糖基转移酶可以将糖残基从活化后的糖基供体转移至各种受体上,UDP-葡萄糖(UDP‑Glc)是糖基化反应的主要供体之一。目前,UDP-葡萄糖已实现商品化生产,但昂贵的价格(1g约1700元)及较差的稳定性是限制UDP-葡萄糖依赖的糖基转移酶进一步发展的主要障碍,使糖基转移酶只能停留于实验室研究水平。探索建立高效合成UDP-葡萄糖的方法势在必行。

目前通常采用酶法或化学法合成UDP-葡萄糖。化学法由于立体选择性较低及过程相 对复杂等因素,不适合行业的长期发展。因此,酶法合成UDP-葡萄糖逐渐成为主流。改造细胞内代谢途径合成UDP‑葡萄糖是研究比较多的一类方法,利用代谢工程改造宿主的UDP-葡萄糖生物合成途径,提高内源性UDP-葡萄糖合成量,并采用全细胞反应与发酵法进行底物的糖基化修饰。
专利CN110699373A改造了大肠杆菌中嘧啶合成途径、改变碳源流量和UDP-葡萄糖的代谢去路,构建了UDP-葡萄糖高产菌株,并验证了其应用的可行性,在完全避免外源性UDP-葡萄糖使用的情况下,UDP-葡萄糖高产大肠杆菌菌株可实现22.5g/L甜茶苷高效合成莱鲍迪苷KA,甜茶苷的转化率达到95.7%。专利CN109371079A以可溶淀粉为主要初始原料,将高温α‑葡聚糖磷酸化酶和高温糖‑1‑磷酸核苷酸化酶分别在大肠杆菌中重组表达,利用表达后的菌体进行高温全细胞催化合成UDP-葡萄糖,省去了酶纯化提取的步骤,节约了时间与成本,简化了操作步骤。但由于全细胞合成的体内代谢网络复杂,反应难操控且产物纯化难度高,产物量偏低。因此,体外一锅法(One‑pot)是目前最为常用的酶法UDP-葡萄糖合成策略。然而,现有一锅法合成UDP-葡萄糖的反应中使用的酶均为常温酶,稳定性较差。嗜热酶的应用可以很好地解决这一问题,成为高效合成UDP-葡萄糖的理想选择。
制备方法[1]
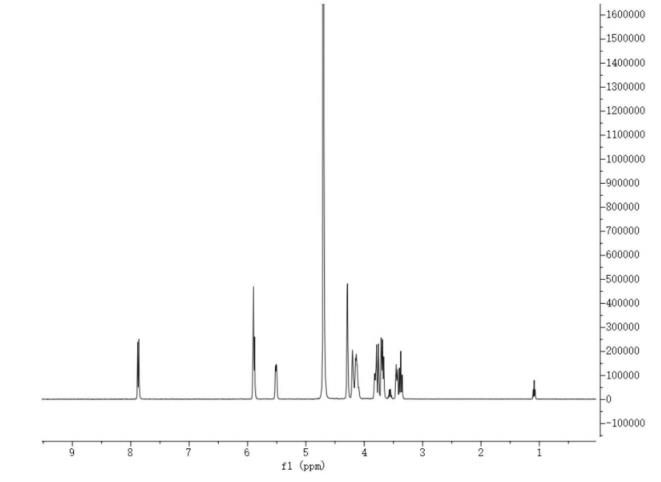
由嗜热葡萄糖激酶GS01513、嗜热磷酸葡萄糖变位酶TTHA0353和嗜热尿苷二磷酸葡萄糖焦磷酸化酶IM867_06155催化合成得到UDP-葡萄糖(GPUP),该一锅法反应包括三个催化过程:(i)以D‑葡萄糖、UTP(尿嘧啶核苷三磷酸)为底物,嗜热葡萄糖激酶GS01513催化合成得到6‑P‑Glc(6‑磷酸‑葡萄糖);(ⅱ)以6‑P‑Glc为底物,嗜热磷酸葡萄糖变位酶TTHA0353催化合成得到1‑P‑Glc(1‑磷酸‑葡萄糖);(iii)以1‑P‑Glc和UTP为底物,嗜热尿苷二磷酸葡萄糖焦磷酸化酶IM867_06155催化合成得到UDP-葡萄糖并产生反应抑制副产物PPi (焦磷酸),同时嗜热无机焦磷酸酶PPase(专利申请号:202110765804.0,核苷酸序列为SEQ ID No.6所示)去除副产物PPi ,提高产物合成效率。
由上述四种酶催化的一锅法偶联反应(GPUP)具体实验流程如下:将UTP和D‑葡萄糖按摩尔比2:1加入到50mM的Na2HPO4 ‑NaOH缓冲液(pH8.0~10.0)中使二者的终浓度分别为50~120mM,再加入终浓度为5~10mM的MgCl2;随后依次加入嗜热葡萄糖激酶GS01513、嗜热磷酸葡萄糖变位酶TTHA0353、嗜热尿苷二磷酸葡萄糖焦磷酸化酶IM867_06155和嗜热无机焦磷酸酶PPase,四种酶的终浓度分别为0.3~0.6mg/mL;最后于50~60℃下以150~200 rpm振荡反应4~6h,沸水浴2~5min终止反应,得到产物UDP-葡萄糖。
参考文献
[1]吉林大学. 嗜热酶及一锅法高效合成UDP-葡萄糖和UDP-葡萄糖醛酸的方法:CN202210140823.9[P]. 2023-11-21.
